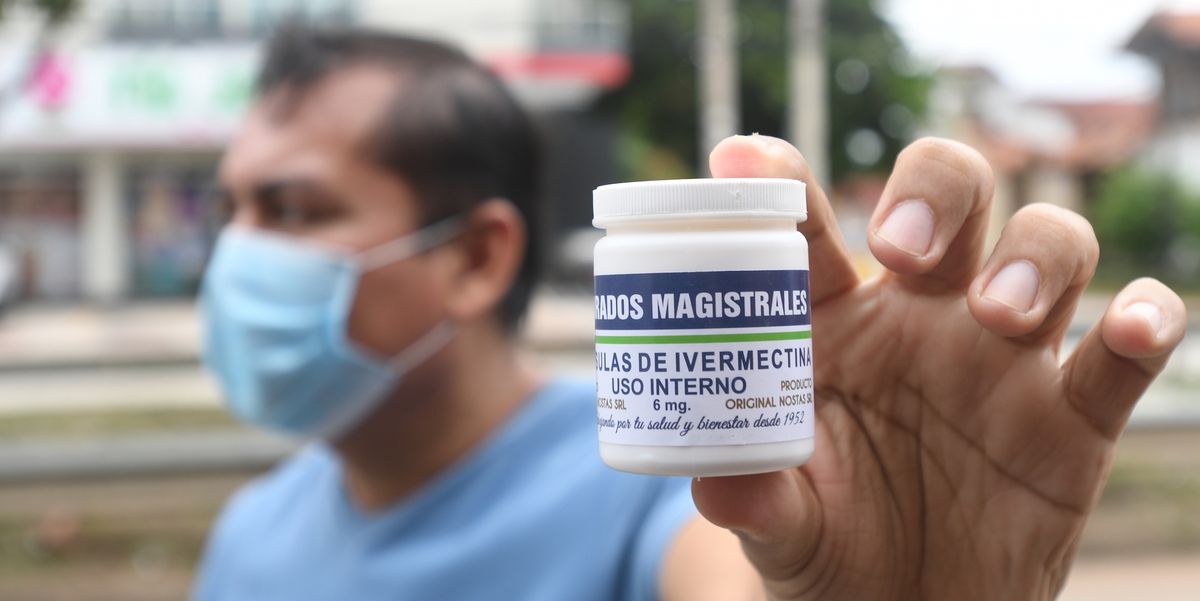
L’ivermectine est un médicament essentiellement
antiparasitaire à spectre large. Certaines études très récentes
menées in vitro démontrent par ailleurs que l’ivermectine
est capable d’inhiber la réplication du SARS-CoV-2 à des
concentrations micromolaires. A cette notion, se sont ajoutées des
études d’observation et des séries de cas qui suggèrent une
efficacité potentielle de ce médicament face à la Covid-19. Des
observations cliniques provenant du Bangladesh et d’Argentine ont
également appuyé la décision d’entreprendre un essai pilote, mais
randomisé et mené à double insu contre placebo. Celui s’est déroulé
dans le centre universitaire de Navarre (Espagne).
Entre le 31 juillet et le 11 septembre 2020, ont été inclus 24
patients atteints d’une forme symptomatique légère de la maladie
révélée par une fièvre et de la toux évoluant depuis moins de 72
heures. Il n’existait aucun facteur de risque pouvant faire
craindre l’évolution vers une forme sévère.
Dans le groupe traité (n = 12), une dose unique d’ivermectine
a été administrée par voie orale et un placebo dans l’autre groupe
(n = 12). Le critère d’efficacité primaire était la proportion de
patients chez lesquels la charge virale estimée par RT-PCR était
non détectable, le test étant effectué sur un prélèvement
nasopharyngé sept jours après l’exposition au médicament. Les
différences entre les groupes ont été évaluées au moyen d’un test
exact de Fisher et calculées sous la forme de risk ratios
(RRs).
Recul plus rapide des troubles de l’odorat et peut-être de la toux
Tous les participants (âge médian 26 ans, écart interquartile
[EIQ] 19–36 dans le groupe ivermectine et 21–44 dans le groupe
témoin ; femmes : 50 %) sont allés jusqu’au terme de l’étude. Au
septième jour de l’évolution, la proportion de tests PCR positifs
était la même dans les 2 groupes, le RR correspondant étant de 0,92
(intervalle de confiance à 95 % IC 95% : 0,77–1,09, NS). La charge
virale s’est avérée un peu plus faible dans le groupe traité sans
que le seuil de signification statistique soit atteint au
4ème (p = 0,24 pour le gène E ; p = 0,18
pour le gène N) comme au 7ème jour (p =
0,16 pour le gène ; p = 0,18 pour le gène N). La même tendance (p
=0,24) a été observée en ce qui concerne les titres d’anticorps IgG
dosés 21 jours après la prise du médicament. Par ailleurs, dans le
groupe traité, l’amélioration de l’anosmie ou de l’hyposmie
rapportée par le patient- a été plus rapide et la différence
intergroupe, dans ce cas, s’est avérée statistiquement
significative (76 versus 158 patients-jours ; p < 0,001).
Une tendance voisine a été observée pour la toux (seuil de
signification statistique non atteint.)
Dr Peter Stratford




