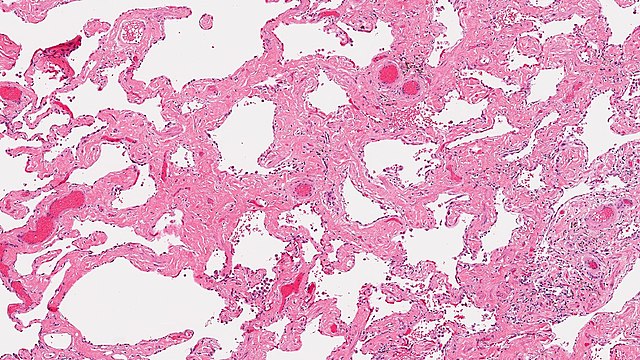
Les pneumopathies interstitielles du fumeur sont des entités complexes qui sont périodiquement mises à jour à la lueur des connaissances nouvelles. Leur haute prévalence chez les fumeurs mérite largement ces actualisations qui permettent en outre de mettre un peu d’ordre dans un contexte touffu.
Ces pneumopathies peuvent être schématiquement classées dans trois groupes :Haut du formulaire
1) Celles liées à l’accumulation de macrophages littéralement empoussiérés au niveau des bronchioles et des alvéoles : il s’agit de la bronchiolite respiratoire (BR), associée ou non à une pneumopathie interstitielle diffuse (BR-PID), mais aussi de la pneumopathie interstitielle desquamative (PIDE)
2) Celles liées à une fibrose interstitielle associée mais prédominante : il s’agit des syndromes dits AEF (Airway Enlargement with Fibrosis) et CPFE (Combined Pulmonary Fibrosis and Emphysema)
3) Celles en rapport avec une néoplasie inflammatoire étroitement associée au tabagisme : l’histiocytose pulmonaire à cellules de Langerhans (HPCL)
Groupe 1 : BR, BR-PID et PIDE
gG cDEDe fait, chez le fumeur même asymptomatique, les lésions inflammatoires des voies aériennes distales sont constantes, le plus souvent à type d’accumulation de macrophages pigmentés dans la lumière des bronchioles respiratoires et d’inflammation chronique péribronchiolaire. Sur le plan de la sémiologie radiologique, les micronodules centrolobulaires en verre dépoli de faible densité siégeant au niveau des lobes supérieurs signent la présence d’une BR.
La BR-PID, pour sa part, correspond à un tableau clinique associant toux chronique et dyspnée d’effort, associées ou non à perturbations modérées des explorations fonctionnelles respiratoires. Il est impossible de différencier histologiquement BR et BR-PID, la clinique permettant de trancher entre l’une et l’autre. La PIDE, pour sa part, correspond à une accumulation intra-alvéolaire de macrophages pigmentés qui finit par prédominer, tout en s’associant à une hyperplasie des pneumocytes de type II. Sa traduction radiologique consiste en l’apparition de plages de verre dépoli extensives, le plus souvent bilatérales et symétriques, qui prédominent toutefois au niveau des lobes inférieurs et en périphérie des champs pulmonaires.
Groupe 2 : AEF et CPFE
Dans ces deux syndromes qui peuvent coexister, c’est la fibrose qui domine le tableau histologique, avec en toile de fond l’emphysème qui est présent chez tous les fumeurs. De fait, l’AEF dite aussi SRIF (Smoking-Related Interstitial Fibrosis) se caractérise par une fibrose interstitielle hyalinisée qui va prédominer dans les régions sous-pleurales des tiers supérieur et moyen des lobes inférieurs.
Sur le plan radiologique, elle se traduit par des images de kystes multiples, plus ou moins volumineux, à parois irrégulières, préférentiellement situés dans les régions sous-pleurales. Il n’existe en règle ni bronchiolectasie par traction ni perte de volume ni rayon de miel : une sémiologie qui permet de distinguer l’AEF de la pneumopathie interstitielle commune dont le pronostic est bien plus réservé.
Le syndrome CPFE (emphysème-fibrose), constitue, pour sa part, une entité nouvelle encore mal connue et débattue qui a fait toutefois l’objet d’un consensus en 2022. Elle combine un emphysème des sommets et une fibrose basale qui évoque la pneumopathie interstitielle commune sans pour autant en partager l’évolution ou le pronostic.
Groupe 3 : l’histiocytose pulmonaire à cellules de Langerhans (HPCL)
L’histiocytose langerhansienne est appartient depuis 2016 aux néoplasies myéloïdes, qui se répartissent en 4 sous-types : (a) unifocale (typiquement le granulome éosinophile) ; (b) l’histiocytose pulmonaire à cellules de Langerhans (PLCH) isolée ; (c) la forme monosystémique multifocale (plus d’une lésion de n’importe quel organe) ; (d) la fome multisystémique. La PLCH est le sous-type le plus fréquemment rencontré chez l’adulte jeune. Son évolution se fait par poussées évolutives avec apparition de micronodules centrolobulaires en verre dépoli appelés à se densifier progressivement. Les nodules de plus en plus denses aboutissent in fine à la formation de kystes de forme et de taille variables, répartis selon un gradient apicobasal assez caractéristique. La présence de lésions d’âges différents à type de nodules solides, mixtes et de kystes est un autre signe caractéristique.
Dr Philippe Tellier




